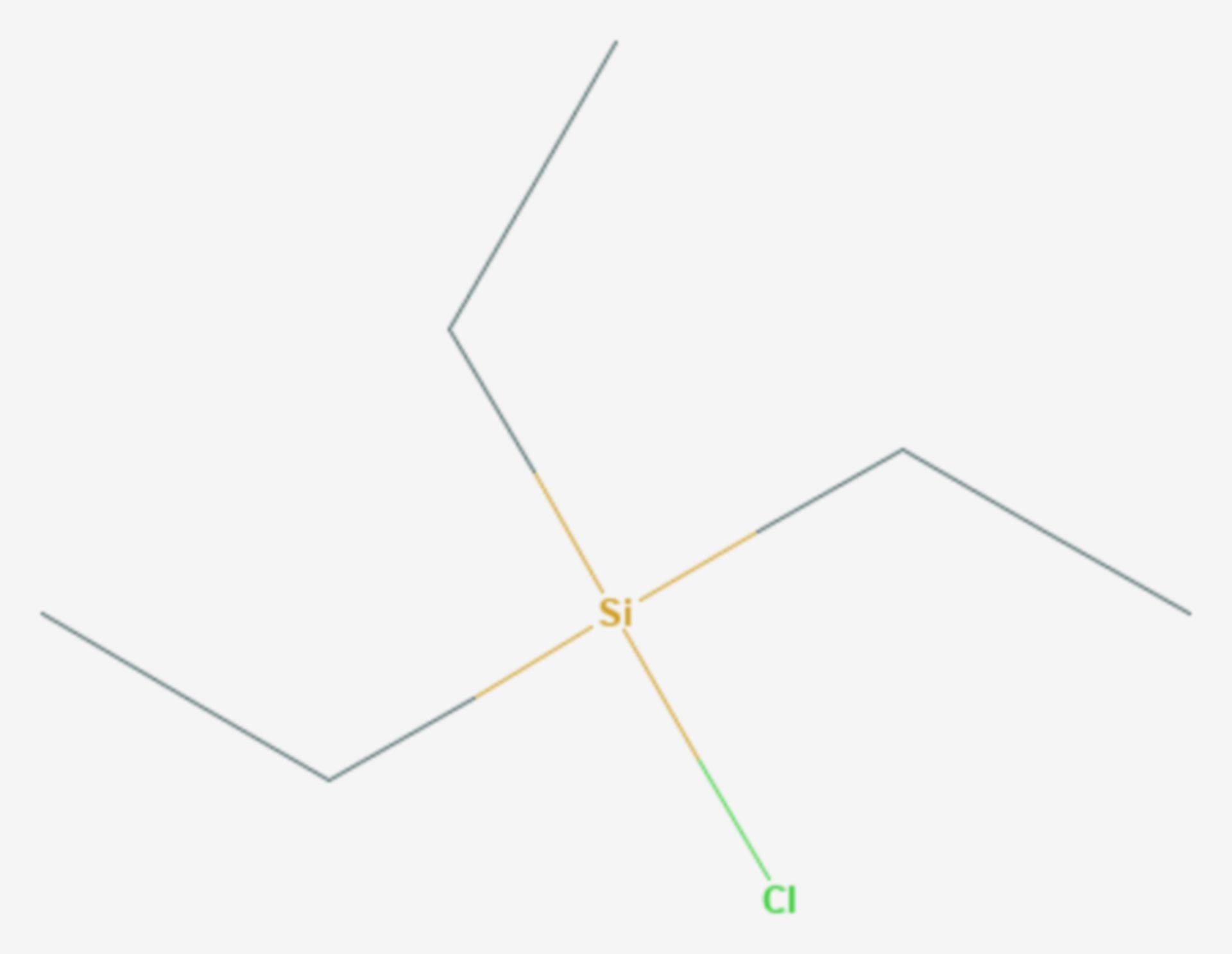
Triethylsilan ist eine chemische Verbindung aus der Gruppe der siliciumorganischen Verbindungen.
Gewinnung und Darstellung
Eine Möglichkeit zur Herstellung von Triethylsilan ist die Hydrierung der entsprechenden Chlorverbindung mit Lithiumaluminiumhydrid oder Natriumhydrid:
Eine andere Möglichkeit ist die Umsetzung von Trichlorsilan mit dem Grignard-Reagenz Ethylmagnesiumbromid in Diethylether:
Eigenschaften
Physikalische Eigenschaften
Triethylsilan ist eine klare, farblose Flüssigkeit mit beißendem, knoblauchartigem Geruch und einem Flammpunkt von −2,99 °C.
Kernspinresonanzspektroskopie-Daten:
Chemische Eigenschaften
Wie andere Silane reagiert auch Triethylsilan mit protischem Wasserstoff wie OH-Gruppen oder Ammoniak unter Bildung von Wasserstoff-Gas zum Triethylsilanol bzw. zum entsprechenden Disilazan:
Verwendung
Triethylsilan hat eine reaktive Silicium-Wasserstoffbindung, daher kann es als Reduktionsmittel u. a. zur Hydrosilylierung von Doppelbindungen in Alkenen, Aldehyden oder Ketonen verwendet werden. Bei der Reaktion mit Alkenen werden Triethylsilylalkane gebildet:
Triethylsilan kann in der präparativen Chemie dazu benutzt werden, um im Alkylchloriden den Chloridliganden durch Wasserstoff zu ersetzen:
Sicherheitshinweise
Der LD50-Wert (oral, Ratte) liegt bei > 2000 mg/kg. Der EC50-Wert (Daphnia magna, „Großer Wasserfloh“) liegt bei 52 mg/l-48 h.
Einzelnachweise